化学中,原子半径大小的比较?离子半径大小的比较?
简单粒子半径比较,从以下四个方面考虑 1原子半径 同周期:主族元素,从左到右,原子半径逐渐减小, 如: 同主族:元素的原子,从上到下,原子半径逐渐增大 2离子半径: 同主族元素的离子,核电荷数越大,离子半径越大 如:Na+ Al3+
元素周期表中、原子半径大小有何规律??
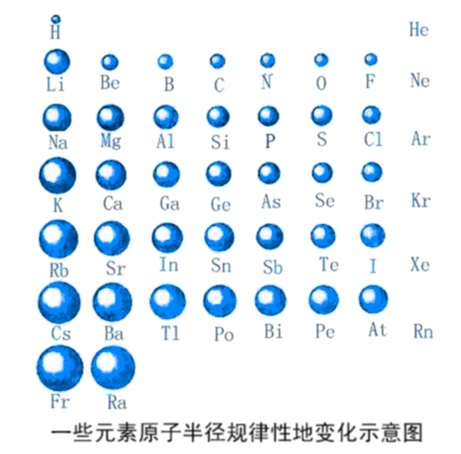
除第1周期外,其他周期元素(稀有气体元素除外)的原子半径随原子序数的递增而减小;
同一族的元素从上到下,随电子层数增多,原子半径增大。(五、六周期间的副族除外) 同一周期内,从左到右,元素核外电子层数相同。
元素周期表中原子半径跟元素序数的关系
元素周期表中原子半径跟元素序数的关系:
主族元素:同主族的,从上到下,半径逐渐变大;(因为电子层数在不断增加)
同周期的,从左到右,半径逐渐变小;(因为质子数增加吸引力越大,半径随之减少)
副族元素半径变化没有规律。
嘛. 就是短周期的那18个元素的原子半径就行了 不要图 就按 Na 0.186 nm 短周期各原子半径大小: 1,H 0.037nm 氢原子即氢元素的原子。氢原子模型是电中性的原子含有一个正价的质子与一个负价的电子,他们被库仑定律束缚于原子核。氢原子是丰度最高的同位素。 2,Li 0.152nm 锂(Li)是一种银白色的金属元素,质软。
化学中元素周期表元素半径大小排列规律
元素半径的大小排列规律是怎样的?谢…
[编辑本段]元素周期表中元素及其化合物的递变性规律 1 原子半径 (1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小; (2)同一族的元素从上到下,随电子层数增多,原子半径增大。
化学原子半径在元素周期表中的比较方法。
化学中,原子半径在同周期或同族中如何比较?还有金属性和非金属性在同同周期(除去稀有气体)从左至右,半径逐渐减小,非金属性逐渐增强 同主族,从上至下,半径逐渐变大,金属性逐渐增强 就是说,越往右上角走,半径越小,非金属性越强,例如:氟 越往左下角走,半径越大,金属性越强。
怎么简单记住化学元素周期表中的原子半径大小,气同周期元素从左到右原子半径变小,因为他们的电子层数相同但越往右原子相对质量越大,电荷越多,对电子的吸引越强,半径就越校 中心原子的氧化性越强,气态氢化物越稳定。一般同族元素从上到下。
所有化学元素的原子半径大小,急。。。。。。
元素周期表中离子半径怎么比较
离子半径大小的判断方法: (1)同一元素的微粒,电子数越多,半径越大。如钠原子>钠离子,氯原子铁离子; (2)同一周期内元素的微粒,阴离子半径大于阳离子半径。如氧离子>锂离子; (3)同类离子与原子半径比较相同。如钠离子>镁离子>铝离子
化学元素周期律总结>>>原子半径大小,金属性和非金有图最好,加分
原子半径 同一周期(稀有气体除外),从左到右,随着原子序数的递增,元素原子的半径递减; 同一族中,从上到下,随着原子序数的递增,元素原子半径递增。 (注):阴阳离子的半径大小辨别规律 由于阴离子是电子最外层得到了电子 而阳离子是失去
本文内容由网友自发贡献,版权归原作者所有,本站不承担相应法律责任。如您发现有涉嫌抄袭侵权的内容,请联系:hwhale#tublm.com(使用前将#替换为@)